30
2022.03
PCR技術大躍進: Blood Direct PCR崛起
近年來Covid-19的全球大爆發、非洲豬瘟的生豬產業重創等氛圍下,分子檢測揭開了其神秘的面紗進入人們的視野中。一方面在疫情期間分子檢測的需求攀升,另一方面是攀升的需求使得各國衛生機構的運行負荷驟增。因此開發快速且精準之核酸檢測技術是各家IVD企業爭相搶奪的高地。
PCR(Polymerase Chain Reaction)技術自1983年發展迄今已成為生命科學領域應用最廣泛、使用頻率最高也最重要的核酸基礎研究手段 。然而,在傳統PCR技術以及在此基礎上衍生出來的各項新技術、新應用如Multi PCR、Digital PCR等都需要事先獲得高純度的核酸模板,使得核酸分離萃取經常是相關科研技術人員需不斷重複的基礎工作。對於有大量樣品需要研究的人員,分離提取核酸則為一項勞動量極大的工作。即便現在市場上核酸分離萃取試劑盒多為成熟且品牌眾多,但無論採用如管柱萃取純化法(Column Purification)或試劑萃取純化法等仍需要大量的操作時間並增加科研、檢驗成本。
血液是一種重要的生物分析樣本,含有極其豐富的有關體內所有組織和器官功能的資訊,對血液樣品進行分析是醫學和科學領域研究關注的焦點。然而,血液樣本含有大量免疫球蛋白、血紅蛋白的血紅素分子等複雜物,以及用於穩定樣本的抗凝血劑(如EDTA、檸檬酸鹽或Heparin),而這些物質卻往往成為PCR實驗的抑制物 (PCR inhibitor),故需要進行DNA核酸萃取及純化步驟來移除抑制物,但卻也在萃取的過程中恐會造成珍貴樣本的流失、人為操作造成的實驗誤差及發生樣品交互汙染的可能性。
不經核酸萃取過程直接進行PCR分析的技術,早在1992年就已被用於微生物領域中: Colony-PCR ,但針對血液樣本富含多種干擾物卻成為直接PCR (Direct PCR)的難關。藉由基因改造技術提升與疫情推波助瀾,現市面上以有多種改造後對於血液樣本抑制物具高度耐受性的聚合酶及其配套的緩衝液體系聯合相應擴增程式來實現快速檢測分析的全血直接PCR (Whole Blood direct PCR)套組,不僅為各家廠商之明星商品也是分子診斷領域最熱門產品。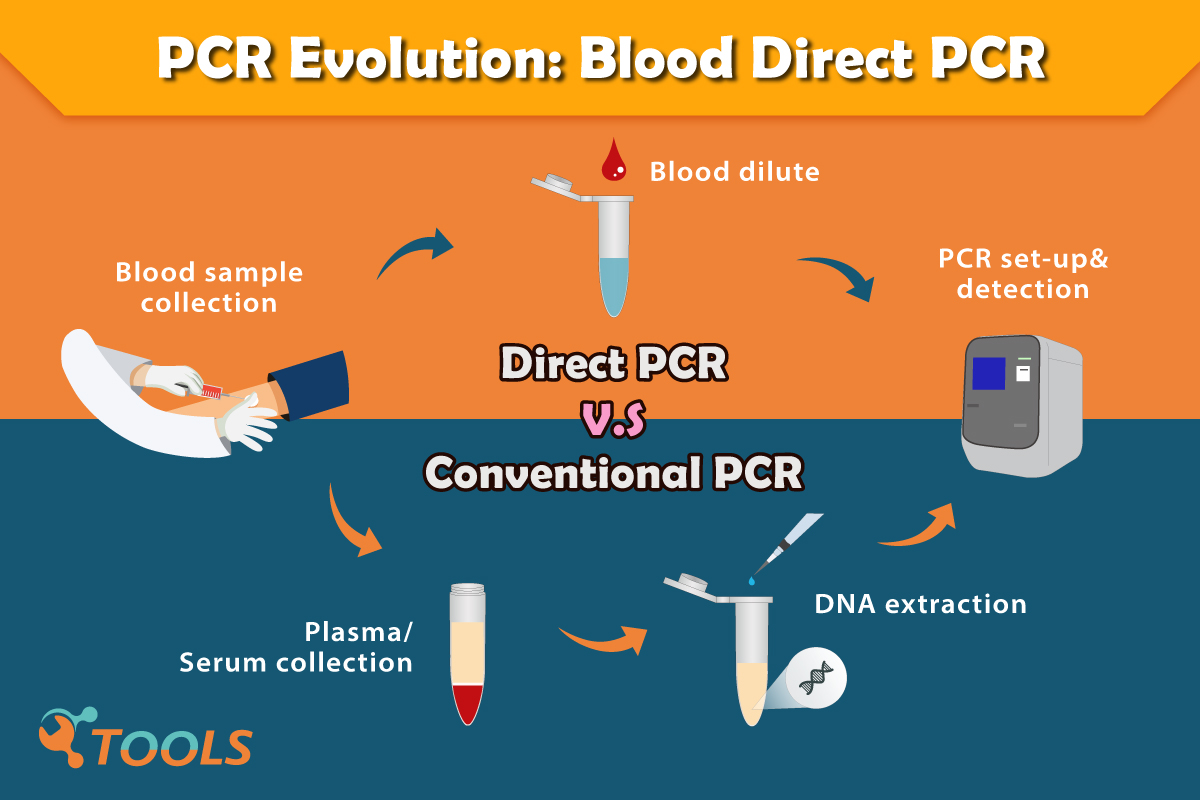
Blood Direct PCR技術具有縮短檢驗時間、提高靈敏度、減少操作步驟和降低污染風險等優點,故可較大程度地節約人力、物力、財力及時間,因而該技術的發展對資料庫建設、重大緊急案件和大規模災難性事故等均有重要的應用價值。如病原體檢測:非洲豬瘟病毒檢測 、HBV病毒檢測 ; 新生兒篩檢 使用微量血液樣本如FTA cards上的乾血漬; 基因分型檢測:PCR-RFLP based SNP (single-nucleotide polymorphism) genotyping ,都提供了簡便、快速但準確的方法。不僅如此,對於基礎科學研究經常使用的轉殖基因鼠(Transgenic mice)之基因分型分析 ,可大幅縮短研究時間與複雜性。更甚,其擴增後之PCR產物亦可直接進行後續應用如Cloning或Sequencing 等。
綜觀前言,Direct PCR技術已是分子檢測的未來趨勢,尤以全血直接PCR在臨床用途上更顯其重要。圖爾思生技致力於成為科學家們最好的夥伴,在研究之路上一直為大家提供最好的研究工具、最佳的原物料。近期更重磅推出新產品:TOOLS BlooDirect PCR kit (#TTG-BP01),便是針對現下最夯的全血直接PCR所自行開發產品。不僅可直接應用在學術研究上,亦可做為專注於IVT檢測試劑開發商之優質原物料試劑。

回上一頁
PCR(Polymerase Chain Reaction)技術自1983年發展迄今已成為生命科學領域應用最廣泛、使用頻率最高也最重要的核酸基礎研究手段 。然而,在傳統PCR技術以及在此基礎上衍生出來的各項新技術、新應用如Multi PCR、Digital PCR等都需要事先獲得高純度的核酸模板,使得核酸分離萃取經常是相關科研技術人員需不斷重複的基礎工作。對於有大量樣品需要研究的人員,分離提取核酸則為一項勞動量極大的工作。即便現在市場上核酸分離萃取試劑盒多為成熟且品牌眾多,但無論採用如管柱萃取純化法(Column Purification)或試劑萃取純化法等仍需要大量的操作時間並增加科研、檢驗成本。
血液是一種重要的生物分析樣本,含有極其豐富的有關體內所有組織和器官功能的資訊,對血液樣品進行分析是醫學和科學領域研究關注的焦點。然而,血液樣本含有大量免疫球蛋白、血紅蛋白的血紅素分子等複雜物,以及用於穩定樣本的抗凝血劑(如EDTA、檸檬酸鹽或Heparin),而這些物質卻往往成為PCR實驗的抑制物 (PCR inhibitor),故需要進行DNA核酸萃取及純化步驟來移除抑制物,但卻也在萃取的過程中恐會造成珍貴樣本的流失、人為操作造成的實驗誤差及發生樣品交互汙染的可能性。
不經核酸萃取過程直接進行PCR分析的技術,早在1992年就已被用於微生物領域中: Colony-PCR ,但針對血液樣本富含多種干擾物卻成為直接PCR (Direct PCR)的難關。藉由基因改造技術提升與疫情推波助瀾,現市面上以有多種改造後對於血液樣本抑制物具高度耐受性的聚合酶及其配套的緩衝液體系聯合相應擴增程式來實現快速檢測分析的全血直接PCR (Whole Blood direct PCR)套組,不僅為各家廠商之明星商品也是分子診斷領域最熱門產品。

Blood Direct PCR技術具有縮短檢驗時間、提高靈敏度、減少操作步驟和降低污染風險等優點,故可較大程度地節約人力、物力、財力及時間,因而該技術的發展對資料庫建設、重大緊急案件和大規模災難性事故等均有重要的應用價值。如病原體檢測:非洲豬瘟病毒檢測 、HBV病毒檢測 ; 新生兒篩檢 使用微量血液樣本如FTA cards上的乾血漬; 基因分型檢測:PCR-RFLP based SNP (single-nucleotide polymorphism) genotyping ,都提供了簡便、快速但準確的方法。不僅如此,對於基礎科學研究經常使用的轉殖基因鼠(Transgenic mice)之基因分型分析 ,可大幅縮短研究時間與複雜性。更甚,其擴增後之PCR產物亦可直接進行後續應用如Cloning或Sequencing 等。
綜觀前言,Direct PCR技術已是分子檢測的未來趨勢,尤以全血直接PCR在臨床用途上更顯其重要。圖爾思生技致力於成為科學家們最好的夥伴,在研究之路上一直為大家提供最好的研究工具、最佳的原物料。近期更重磅推出新產品:TOOLS BlooDirect PCR kit (#TTG-BP01),便是針對現下最夯的全血直接PCR所自行開發產品。不僅可直接應用在學術研究上,亦可做為專注於IVT檢測試劑開發商之優質原物料試劑。

-
了解產品資訊 TOOLS BlooDirect PCR kit
Reference
1. Bartlett JM, Stirling D. A short history of the polymerase chain reaction. Methods Mol Biol. 2003;226:3-6. doi: 10.1385/1-59259-384-4:3. PMID: 12958470.
2. Ward AC. Rapid analysis of yeast transformants using colony-PCR. Biotechniques. 1992 Sep;13(3):350. PMID: 1389166.
3. Elnagar A, Harder TC, Blome S, Beer M, Hoffmann B. Optimizing Release of Nucleic Acids of African Swine Fever Virus and Influenza A Virus from FTA Cards. Int J Mol Sci. 2021 Nov 29;22(23):12915. doi: 10.3390/ijms222312915. PMID: 34884719; PMCID: PMC8657678.
4. Astbury S, Costa Nunes Soares MM, Peprah E, King B, Jardim ACG, Shimizu JF, Jalal P, Saeed CH, Sabeer FT, Irving WL, Tarr AW, McClure CP. Nanopore sequencing from extraction-free direct PCR of dried serum spots for portable hepatitis B virus drug-resistance typing. J Clin Virol. 2020 Aug;129:104483. doi: 10.1016/j.jcv.2020.104483. Epub 2020 Jun 2. PMID: 32544862.
5. Takeuchi A, Tode C, Nishino M, Wijaya YOS, Niba ETE, Awano H, Takeshima Y, Saito T, Saito K, Lai PS, Bouike Y, Nishio H, Shinohara M. Newborn Screening for Spinal Muscular Atrophy: DNA Preparation from Dried Blood Spot and DNA Polymerase Selection in PCR. Kobe J Med Sci. 2019 Nov 14;65(3):E95-E99. PMID: 32029694; PMCID: PMC7012323.
6. Kim SW, Heo JH, Kim CH, Yoo DC, Won DH, Lee SG, Cho KJ, Song JH, Park SJ, Yang YG, Choi DW. Rapid and direct detection of apolipoprotein E genotypes using whole blood from humans. J Toxicol Environ Health A. 2010;73(21-22):1502-10. doi: 10.1080/15287394.2010.511573. PMID: 20954076.
1. Bartlett JM, Stirling D. A short history of the polymerase chain reaction. Methods Mol Biol. 2003;226:3-6. doi: 10.1385/1-59259-384-4:3. PMID: 12958470.
2. Ward AC. Rapid analysis of yeast transformants using colony-PCR. Biotechniques. 1992 Sep;13(3):350. PMID: 1389166.
3. Elnagar A, Harder TC, Blome S, Beer M, Hoffmann B. Optimizing Release of Nucleic Acids of African Swine Fever Virus and Influenza A Virus from FTA Cards. Int J Mol Sci. 2021 Nov 29;22(23):12915. doi: 10.3390/ijms222312915. PMID: 34884719; PMCID: PMC8657678.
4. Astbury S, Costa Nunes Soares MM, Peprah E, King B, Jardim ACG, Shimizu JF, Jalal P, Saeed CH, Sabeer FT, Irving WL, Tarr AW, McClure CP. Nanopore sequencing from extraction-free direct PCR of dried serum spots for portable hepatitis B virus drug-resistance typing. J Clin Virol. 2020 Aug;129:104483. doi: 10.1016/j.jcv.2020.104483. Epub 2020 Jun 2. PMID: 32544862.
5. Takeuchi A, Tode C, Nishino M, Wijaya YOS, Niba ETE, Awano H, Takeshima Y, Saito T, Saito K, Lai PS, Bouike Y, Nishio H, Shinohara M. Newborn Screening for Spinal Muscular Atrophy: DNA Preparation from Dried Blood Spot and DNA Polymerase Selection in PCR. Kobe J Med Sci. 2019 Nov 14;65(3):E95-E99. PMID: 32029694; PMCID: PMC7012323.
6. Kim SW, Heo JH, Kim CH, Yoo DC, Won DH, Lee SG, Cho KJ, Song JH, Park SJ, Yang YG, Choi DW. Rapid and direct detection of apolipoprotein E genotypes using whole blood from humans. J Toxicol Environ Health A. 2010;73(21-22):1502-10. doi: 10.1080/15287394.2010.511573. PMID: 20954076.



