26
2022.01
Synthetic mRNA:金鑰傳遞者


mRNA在新冠疫情中異軍突起,成為炙手可熱的治療開發方向,目前在臨床用途主要集中在傳染病的疫苗、取代蛋白質或DNA進行基因治療遺傳性疾病或癌症。然而開發mRNA作為一種治療手段也面臨著與任何藥物投遞相同的挑戰:穩定性與傳遞。
首先mRNA依然可能激發急性免疫反應,進而被清除,無法有效地發揮功能。雙鏈和單鏈RNA與檢測病原體相關的模式識別受體(pattern-recognition receptors, PRRs), 如包括Toll-like receptor(TLRs)相互結合,隨後通過MyD88和TRIF等下游信號傳遞啟動了細胞發炎反應1, 2。
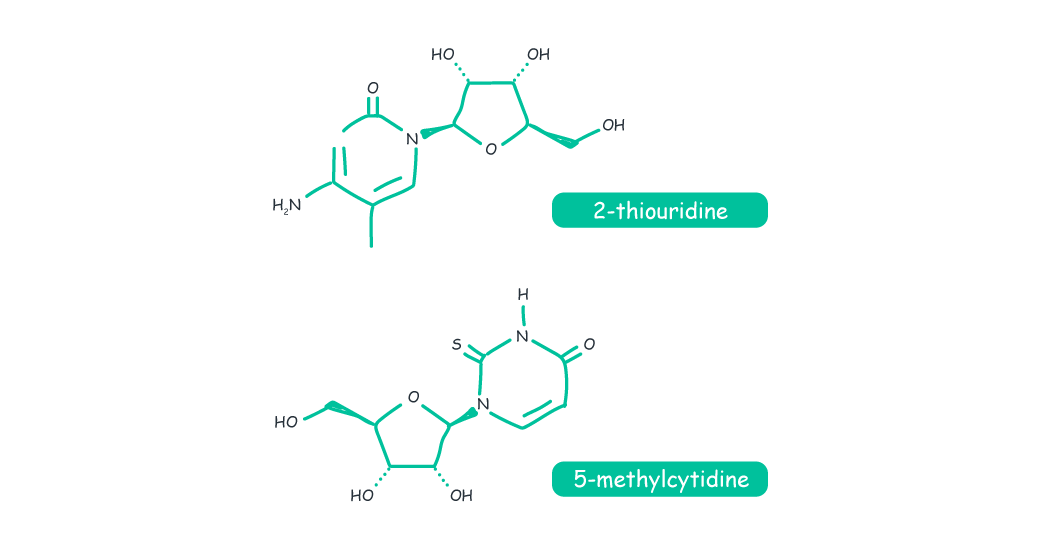
Kormann et al.證實帶有修飾核苷酸類似物的mRNA,例如2-thiouridine與 5-methylcytidine可以阻止TLR的信號傳遞,降低受mRNA刺激的樹突狀細胞 (dendritic cell, DC) 其細胞激素的表達量3。另也發現2-thiouridine與 5-methylcytidine可抑制mRNA與TLR 3、7、8以及視黃醇誘導基因-1產物(retinoid-inducible gene-1 produc,另一種PRR)的接觸,並可抑制已轉染mRNA之血液單核細胞中的細胞激素,例如:干擾素IFN-g和IFN-a,以及白細胞介素-12(IL-12)的表達。修飾核苷酸類似物有效地被抑制mRNA所引發的急性免疫反應,增加mRNA於體內的穩定性。
Kormann et al.證實帶有修飾核苷酸類似物的mRNA,例如2-thiouridine與 5-methylcytidine可以阻止TLR的信號傳遞,降低受mRNA刺激的樹突狀細胞 (dendritic cell, DC) 其細胞激素的表達量3。另也發現2-thiouridine與 5-methylcytidine可抑制mRNA與TLR 3、7、8以及視黃醇誘導基因-1產物(retinoid-inducible gene-1 produc,另一種PRR)的接觸,並可抑制已轉染mRNA之血液單核細胞中的細胞激素,例如:干擾素IFN-g和IFN-a,以及白細胞介素-12(IL-12)的表達。修飾核苷酸類似物有效地被抑制mRNA所引發的急性免疫反應,增加mRNA於體內的穩定性。
圖爾思攜手國際核酸大廠TriLink提供多種核苷酸類似物修飾,可供做於In vitro transcription的原料;亦提供相關客製合成的服務,滿足所有對mRNA的開發與研究需求。
除了通過mRNA本身的核酸修飾來增加穩定性,高效率的體內mRNA傳遞材料與系統對實現治療相同地至關重要。外源mRNA必須穿透脂質膜的屏障,才能到達細胞質,轉化為功能性蛋白質,mRNA的吸收機制與細胞類型極為相關,mRNA複合物的理化性質則可深刻影響其傳遞效率和可到達分佈的器官。
曾經,傳遞mRNA至細胞的基本方法有兩種:第一,將mRNA載入到體外培植的細胞中,然後將已接受mRNA的細胞回輸於體內4,可精確控制細胞目標、轉染效率和其他細胞條件,但昂貴和勞動密集;第二,直接於目標位置注射mRNA,無論是否具有運輸載體,但無法精確和有效的進行特異性傳遞。為了結合兩種傳遞方式的優點,各種載體分子的開發相應而出5:mRNA與帶正電荷的水包油陽離子奈米乳狀物(A)。mRNA與化學修飾的樹枝狀聚合物和聚乙二醇(PEG)脂質複合物(B);PEG-脂質奈米粒子中的原胺(protamine)複合mRNA(C);mRNA與陽離子聚合物如聚乙二醇(PEI)相關(D);與陽離子聚合物如PEI和脂質成分相關的mRNA(E);以多糖(例如殼聚糖)顆粒或凝膠包覆的mRNA(F)。陽離子脂質奈米顆粒(例如:1,2-二油醯氧基-3-三甲基銨丙烷(DOTAP)或二油醯磷脂醯乙醇胺(DOPE))中的mRNA(G);與陽離子脂質和膽固醇複合的mRNA(H);以及與陽離子脂質、膽固醇和PEG-脂質複合的mRNA(I)。

圖爾思攜手美國最專業的聚乙二醇試劑供應商



想與圖爾思一起聊mRNA,就趕快與我們聯絡吧 !




